《基因组研究》杂志:世界上最常见的肝病“非酒精性脂肪肝”的触发因素被确定
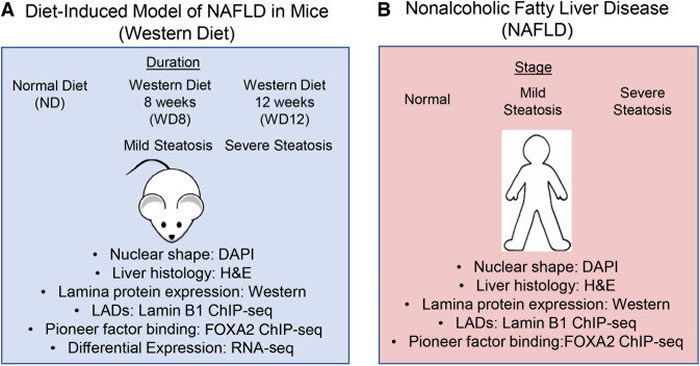
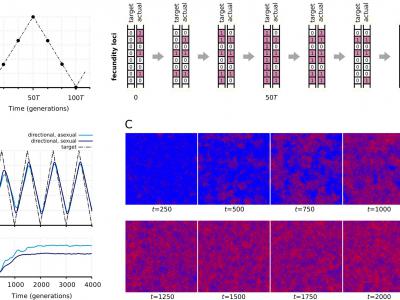
(A)我们使用了饮食诱导的NAFLD小鼠模型(Asgharpour等人,2016年)。给杂合的8-12周龄的C57BL/6J (B6)/129S1/SvImJ (S129)小鼠喂食西方饮食(WD;42%千卡热量来自脂肪,含0.1%胆固醇;Harlan TD.88137)随意消耗葡萄糖和果糖(SW;23.1克/升d-果糖+18.9克/升d-葡萄糖)持续8周(WD8)和12周(WD12),此时动物分别出现轻度和重度脂肪变性。通过DAPI染色确定细胞核形状,通过苏木精-伊红(H&E)染色确定肝脏组织学,通过蛋白质印迹确定叶片蛋白的表达。Lamin B1和FOXA2 ChIP-seq用于鉴定LADs和先锋因子结合。通过RNA-seq测定不同饮食上的差异表达。(B)来自供体的肝组织样品(三个健康,三个具有轻度脂肪变性的NAFLD,和三个具有严重脂肪变性的na fld;健康,26-45岁;NAFLD,21-51岁)从Sekisui XenoTech生物银行获得。通过DAPI染色确定细胞核形状,通过H&E染色确定肝脏组织学,通过western blot确定叶片蛋白的表达。Lamin B1和FOXA2 ChIP-seq用于鉴定LADs和先锋因子结合。Credit: Genome Research (2022). DOI: 10.1101/gr.277149.122
(蜘蛛网eeook.com)据by Josh Barney, University of Virginia:弗吉尼亚大学医学院的研究人员发现了非酒精性脂肪性肝病的关键触发因素,这是一种神秘的疾病,导致脂肪在肝脏中堆积,原因不明。新的见解有助于解释年轻人的情况,并可能导致世界上最常见的肝病的第一种治疗方法。
罪魁祸首?皱纹在包含我们DNA的细胞间隔中形成。弗吉尼亚大学科学家先前的研究表明,这些褶皱的细胞核可能与常见的代谢疾病有关,如糖尿病和脂肪肝疾病,甚至衰老本身。新的结果支持了这些发现,并可能导致针对皱纹的治疗,以阻止脂肪肝疾病,并可能减缓或逆转衰老。
“我们发现了一种涉及细胞核和核纤层的共同机制,这种机制导致患有非酒精性脂肪性肝病的老年人和年轻人肝脏中的脂肪积累,”弗吉尼亚大学药理学部门的高级研究员伊琳娜・m・博奇基斯博士说。“我们的发现可能会导致新的治疗方法,旨在恢复核纤层的功能,以控制异常基因,并逆转非酒精性脂肪性肝病年轻患者或老年人的脂肪肝。”
了解非酒精性脂肪性肝病
脂肪性肝病在大量饮酒的人群中很常见――肝脏中脂肪的过量储存是一个人大量饮酒的危险信号。但是非酒精性脂肪性肝病会侵袭那些很少喝酒或根本不喝酒的人,尤其是老年人和二型糖尿病患者。大约40%的70岁以上的人患有这种疾病。
对许多人来说,脂肪性肝病没有任何症状。他们甚至可能没有意识到自己有这种能力。但对其他人来说,它会导致虚弱、疲劳和腹痛,降低生活质量。不幸的是,没有治疗方法。
医生们一直难以理解是什么引发了非酒精性脂肪性肝病,但UVA的新发现表明,这可能是由包含我们细胞操作指令的“硬盘驱动器”内部的故障造成的,至少部分是如此。这些变化始于储存我们染色体的细胞核,并改变某些基因的活性――最终导致脂肪在肝脏中积累。
新的研究表明,断层开始于细胞核中被称为薄片的部分。核膜层充当核膜和核膜内包含的遗传物质(称为染色质)之间的系绳。Bochkis和她的团队发现,薄层中皱纹的形成会影响控制脂肪储存的基因的活性。当这些基因变得过度活跃时,肝脏就会充满多余的脂肪,导致非酒精性脂肪性肝病。
为了验证他们的发现,研究人员观察了从年龄在21-51岁的非酒精性脂肪肝患者中收集的肝细胞。科学家们发现了他们所期望的:褶皱叶片。研究人员说,这有助于解释为什么这种疾病可以袭击任何年龄的人,并且应该有助于识别那些处于危险中的人。
通过针对薄层中的有害变化,研究人员可能能够开发出治疗甚至预防非酒精性脂肪性肝病(以及可能的其他代谢疾病甚至衰老)的方法。例如,Bochkis说,科学家可能能够使用定制的病毒将不同的核纤层蛋白输送到肝脏,以平滑细胞膜的表面,并使细胞恢复正常功能。
“目前没有治疗非酒精性脂肪性肝病的方法,也没有对患者进行分层的方法,”Bochkis说。“我们的发现可能会导致分层的改善和一种没有副作用的新治疗方法,在这种方法中,恢复薄层功能可以使细胞恢复到具有适当基因表达的健康状态。”
这项研究发表在《基因组研究》杂志上。
相关:发现严重非酒精性脂肪性肝病的可能遗传基础和小鼠模型
(蜘蛛网eeook.com)据by Liz Ahlberg Touchstone, University of Illinois at Urbana-Champaign:伊利诺伊大学香槟分校的研究人员发现,突变或受损的基因可能是一种严重、神秘的非酒精性脂肪性肝病的原因。研究人员发现,缺乏SRSF1基因的小鼠和人类肝细胞表现出非酒精性脂肪性肝炎(也称为NASH)的所有特征。
伊利诺伊州生物化学教授Auinash Kalsotra说,这种独特的小鼠模型捕捉到了肝脏中多余脂肪、炎症和疤痕的所有三个特征,为更好地理解和开发NASH的治疗方法打开了大门。研究人员将他们的结果发表在《自然通讯》杂志上。
根据美国国立卫生研究院(National Institutes of Health)的数据,估计有25%的美国人患有非酒精性脂肪性肝病,多达三分之一的患者也会出现炎症和疤痕,这属于纳什分类。
“现在还不清楚为什么某些人最终会患上NASH,”卡尔索特拉说。“到目前为止,还没有任何基因与纳什直接相关。这被认为是一个进展:在肝脏受伤或变得肥胖后,如果你不检查它,它将向NASH发展。但并不是每个脂肪肝患者都会患上NASH,而且似乎是随机的,所以为什么会发生这种情况非常令人困惑。”
卡尔索特拉说,另一个使纳什研究变得困难的问题是缺乏好的动物或细胞模型。虽然一些模型结合了一两种症状,然后施加其他损伤来模拟NASH患者的情况,但它们并没有给出该疾病的准确描述。
Kalsotra的小组开始研究SRSF1,一种在细胞中协助剪接RNA的蛋白质,以研究其剪接活性。他们培育了一系列缺乏该基因的小鼠来学习其剪接活性。这些老鼠很快就自发地出现了NASH的所有症状。
“我们看到这个非常兴奋,因为我们认为,这可能是这种疾病的模型。但首先,我们必须弄清楚为什么SRSF1与肝病相关的机制,”该研究的第一作者研究生Waqar Arif说。
研究人员发现,该机制与最初认为的SRSF1的剪接活性无关,而是因为它在DNA解链过程中保护肝脏免受DNA损伤,因此其代码可以转录成RNA。没有SRSF1蛋白,肝细胞开始关闭。
“发生的情况是,由于DNA发生了大范围的损伤,细胞想要死亡。但是它没有能量进行常规的程序性细胞死亡过程。损害如此严重,以至于一切都停止了,”卡尔索特拉说,他也是伊利诺伊州卡尔・r・沃斯基因组生物学研究所和癌症中心的成员。
卡尔索特拉说,这与之前假设的途径相反。不是多余的脂肪导致细胞损伤,而是细胞损伤首先出现,脂肪堆积是因为细胞不能履行其包装消化脂肪的功能。随着免疫系统试图清除死亡和垂死的细胞,炎症加剧,然后纤维化出现,因为死亡组织的斑块上形成了疤痕,试图将肝脏保持在一起。研究人员在没有SRSF1的小鼠和缺乏SRSF1的人类肝细胞系中都发现了相同的序列。
“这些发现告诉我们,肝细胞的基因组必须得到适当的维护,”卡尔索特拉说。“肝细胞比我们身体中的任何其他细胞都更容易受到毒素和DNA损伤。这项研究表明,当肝细胞遇到过度的DNA损伤时,就会出现这些NASH症状。SRSF1对此起着保护作用。它充当肝脏基因组的守护者。”
研究人员希望这些小鼠将有助于其他研究NASH的研究人员,既有助于了解该疾病,也有助于探索潜在的治疗目标。
“我们想看看是否在某些情况下,人类肝脏或其他动物的SRSF1以某种方式失活,”Kalsotra说。“例如,可能有一些毒素或药物或其他环境污染物会导致SRSF1基因失活。弄清楚导致SRSF1沉默的触发因素可以指出治疗目标,以及是否可以在这里应用像抗癌药物这样的防止DNA损伤的东西。有趣的是,许多NASH患者也会患上癌症。这与DNA损伤有关吗?”
研究人员还计划探索其他基因是否以这种方式保护DNA,以及对其中任何一个基因的损害是否也会导致NASH病理。